EL DESAFÍO GLOBAL DE LAS FUMONISINAS
Las fumonisinas son un grupo de micotoxinas producidad por diversos tipos de hongos, fundamentalmente del género Fusarium, siendo las especies más frecuentes F. verticilioides y F. proliferatum. Estos contaminantes representan un riesto significativo para la seguridad alimentaria y la salud pública, ya que su presencia es frecuente en cultivos básicos como el arroz, el sorgo y, de manera especialmente relevante, el maíz y sus derivados (Zhou et al., 2025; Anumudu et al., 2024; Yli-Matilda y Sundheim, 2022)
Dado que los hongos productores de fumonisinas crecen en un amplio rango de temperaturas, pero requieren una alta actividad de agua, estas toxinas se forman generalmente antes de la cosecha o en las primeras etapas del alamacenamientos. Además, estas sustancias son termoestables, por lo que su elevada prevalencia een los piensos es un factor de riesgo significativo (EFSA, 2025; Schaarschmidt y Faulhl-Hassek, 2021).
Características químicas de las fumonisinas
Entre los distintos tipos de fumonisinas identificados se encuentra la serie B. Dentro de esta, la fumonisina B1 (FB1), la fumonisina B2 (FB2) y la fumonisina B3 (FB3) han sido las mayormente estudiadas, sinedo la FB1 la más destacada por su elevada prevalencia y toxicidad (EFSA, 2022; Torre-Hernández et al., 2014). Desde el punto de vista químico, las fumonisinas son diésteres estructuralmente similares que contienen polioles y ácidos tricarboxílicos de glicerol, que se caracterizan por se altamente polares y solubles en agua (Figura 1). Su estructura se asemeja a la de la esfingosina (So) y la esfingosina (Sa), por lo que se clasifican como micotoxinas tipo esfingosina. Estos compuestos son componentes clave de la esfingomielina, un lípido esencial de las membranas celulares implicado en porcesos fundamentales como la proliferación, diferenciación, apoptosis, senescencia y carcinogenésis, además de la interacción y el reconocimiento célula-célula (Lassallette et al., 2025; Qu et al., 2022).
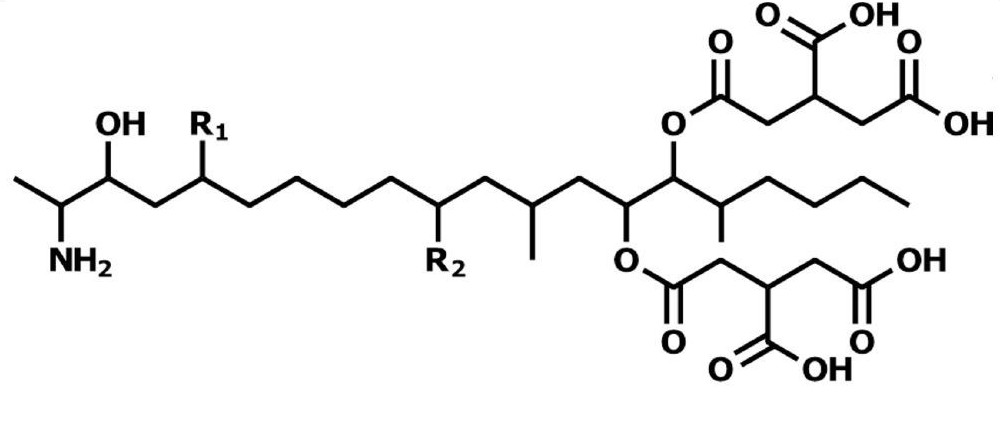
Imágen 1: Estructura química genérica de las fumonisinas del grupo B (Torre - Hernández et al., 2014).
La similitus estructural de las fumonisinas con So y Sa explica su principal mecanismo de toxicidad: la alteración del metabolismo de los esfingolípidos. En este contexto, el ratio Sa:So es ampliamente como biomarcador de exposición a las fumonisinas en las diferentes especies animales (EFSA, 2018)
Prevalencia mundial: un desafío real
En los últimos años, diversas investigaciones han corroborado que la contaminación por fumonisinas en cereales y piensos representa un desafío a nivel mundial. Al respecto, Farhadi et al. (2021) relaizaron una revisión sistemática y un metaanálisis de miles de muestras de alimentos basados en cereales, recolestadas entre 1990 y 2020. Identificando una prevalencia significativa de fumonisinas en múltiples regiones, con una alta concentración en aquello productos derivados del maíz. En concordancia con estos hallazgos, el estudio global de dies años publicado por Gruber-Dorninger et al. (2019) reveló que el 88% de los piensos analizados contenían al menos una micotoxina, destacando las fuminisinas por su alta prevalencia (60%), afectando de nuevo con particular severidad al maíz, el cual presentó una incidencia del 80%.
De manera consistente, encuestas globales de micotoxinas, reportan que la presencia de fumonisinas supera el 60-70% de las muestras analizadas, tanto en materias primas como alimentos balanceados para animales, con variaciones por región geográfica e influencias climáticas (Lopes et al., 2023; Akello et al., 2021; Cheng et al., 2002).
Toxicocinética y toxicidad de las fumonisinas
En cuanto a su toxicocinética, en términos generales, las fumonisinas presentan una baja biodisponibilidad, atribuida principalmente a su estructura cargada (con tres cargas negativas) y a la probable escasa expresión de transportadores específicos a nivel intestinal (EFSA, 2018; Shier, 2000). Sin embargo, a pesar de la baja absorción reportada, estos contaminantes y sus metabolitos generan toxicidad a nivel sistémico, con repercusiones tanto a nivel clínico como subclínico.
Respecto a su metabolización, si bien se han descrito diferencias cualitativas y cuantitativas entre especies, estas micotoxinas suelen experimentar reacciones hidrolíticas secuenciales que tienen lugar principalmente en el tracto gastrointestinal, originando inicialmente fumonisinas A y B parcialmente hidrolizadas (pHF1a y pHF1b) y, posteriormente, HFB₁ (también denominado aminopentol, AP). En los animales expuestos, tanto el compuesto original como sus metabolitos pueden detectarse en hígado y riñón y, en menor medida, en tejido muscular (Anumudu et al., 2024; Qu et al., 2022).
La excreción de estas toxinas se produce mayoritariamente por vía fecal, siendo la excreción urinaria considerablemente inferior (Knutsen et al., 2018 Hartinger et al., 2011; Guerre et al., 2022). Además, se ha reportado el carry-over de las fumonisinas, en productos de origen animal como los huevos o la carne (Osaili et al., 2022; Dazuk et al., 2020).
La toxicidad de las fumonisinas se fundamenta principalmente en la inhibición de la enzima ceramida sintasa, lo que altera la biosíntesis de esfingolípidos y provoca una acumulación de esfinganina, que compromete el crecimiento celular y la señalización del tejido nervioso. Este mecanismo se complementa con la inducción de estrés oxidativo y citotoxicidad, derivando en daños tisulares severos y hepatotoxicidad. De esta forma, las micotoxinas conducen a estados de inmunosupresión y desencadenan problemas gastrointestinales, que derivan en peores rendimientos productivos (Qu et al., 2022; Kulcsár et al., 2023).
La sensibilidad a los efectos de las fumonisinas varía notablemente entre especies; mientras que equinos y porcinos son altamente susceptibles y desarrollan síndromes específicos como la leucoencefalomalacia equina y el edema pulmonar porcino, las aves de corral muestran una mayor resistencia relativa, aunque la exposición crónica sigue impactando su rendimiento productivo, salud intestinal y respuesta inmunológica. Además, el riesgo sanitario se agrava por la frecuente coocurrencia de fumonisinas con otras micotoxinas como deoxinivalenol, zearalenona y aflatoxinas en los alimentos, generando interacciones sinérgicas o aditivas que potencian la toxicidad, tal como se observa en el incremento de lesiones hepáticas y efectos cancerígenos al combinarse con aflatoxina B1 (Anumudu et al., 2024; Guerre et al., 2022; Qu et al., 2022).
BIŌNTE® QUIMITŌX® PLUS: ESTRATEGIA DE MITIGACIÓN DE LAS FUMONISINAS
En este contexto surge BIŌNTE® QUIMITŌX® PLUS como una estrategia eficiente frente a las fumonisinas, con una formula basada en tres modos de acción: adsorción, bioprotección y efecto postbiótico. En primer lugar, su fórmula incluye una mezcla de arcillas seleccionadas de gran calidad, altamente efectivas en la adsorción de fumonisinas, ya que actúan a través de dos tipos de interacciones: interacciones polares con los cationes superficiales, y formación de complejos organometálicos (micotoxina-arcilla) con los centros magnesio estructurales.
Por otro lado, BIŌNTE® QUIMITŌX® PLUS contiene dos ingredientes fitogénicos clave en la mitigación de la toxicidad de las fumonisinas: la curcumina y la silimarina. La curcumina actúa mitigando la toxicidad celular al reducir la acumulación de esfingolípidos y restaurar el equilibrio del calcio intracelular, alterado por las fumonisinas. Además, se ha demostrado su potente efecto hepatoprotector y antioxidante. Complementariamente, la silimarina funciona como un citoprotector directo que reduce significativamente la muerte celular (apoptosis) en los hepatocitos, mediante un mecanismo molecular que implica la regulación de la respuesta inflamatoria y la modulación del daño en el tejido hepático (He et al., 2004; Ledur et al., 2020).
Finalmente, BIŌNTE® QUIMITŌX® PLUS incluye levadura hidrolizada y pared celular de levadura. Por un lado, los β-glucanos y la manano-oligosacáridos, presentes en la pared celular, contribuyen a la captura de micotoxinas en el tracto gastrointestinal (Compagnollo et al., 2020; Elnaggar et al., 2014). Además, estos ingredientes fortalecen la barrera intestinal y estimulan el crecimiento de bacterias beneficiosas en el intestino, lo que mejora la digestión, la absorción de nutrientes y la degradación microbiana de las fumonisinas. Adicionalmente, se ha demostrado que los β-glucanos ejercen un efecto inmunomodulador, reforzando la respuesta del sistema inmune frente a infecciones y al estrés producido por las micotoxinas (Patterson et al., 2023; Pascual et al., 2020).
BIŌNTE® QUIMITŌX® PLUS DEMUESTRA SU EFICACIA EN CONDICIONES IN VITRO E IN VIVO
Esta solución de triple acción ha demostrado su eficacia en condiciones in vitro en estudios llevados a cabo por el Laboratorio de Trilogy, en Estados Unidos. BIŌNTE® QUIMITŌX® PLUS demostró una alta eficacia en la absorción in vitro de un amplio rango de micotoxinas, incluyendo micotoxinas de tipo emergente y modificadas. En concreto, respecto a las fumonisinas, el producto alcanzó una absorción de más del 78% para la FB1, y en torno al 90% para la FB2 y FB3. Registrándose además un porcentaje mínimo de desorción, de aproximadamente el 0.2%, en todos los casos. Estos resultados in vitro se han visto respaldados por pruebas in vivo realizadas en las diferentes especies terrestres.
Eficacia de BIŌNTE® QUIMITŌX® PLUS frente a las fumonisinas en aves
En primer lugar, fue realizado un estudio toxicocinético en aves con la Universidad de Gante (Bélgica), para evaluar la capacidad de adsorción de la FB1 en estos animales. En el caso de los pollos de engorde, la absorción de esta micotoxina es significativamente rápida en la porción proximal del intestino delgado, por lo que su presencia en sangre puede detectarse en un corto periodo de tiempo tras la ingesta del alimento contaminado (Antonissen et al., 2020). Es por ello que resulta esencial garantizar una acción rápida de los productos anti-micotoxinas, con el fin de evitar la llegada de la FB1 a la sangre, y con ello su distribución y toxicidad a nivel orgánico.
En este ensayo, BIŌNTE® QUIMITŌX® PLUS demostró su elevada eficacia transcurridos 5 minutos desde su administración. Su suplementación dio lugar a una reducción de un 74% en la concentración máxima de FB1 detectada en el plasma de los animales; además de reducir en un 82% la biodisponibilidad total de esta micotoxina (Figura 1). De esta forma, se confirma que el producto reduce significativamente la llegada de la micotoxina y sus metabolitos a la circulación sistémica, protegiendo así la salud de los animales.
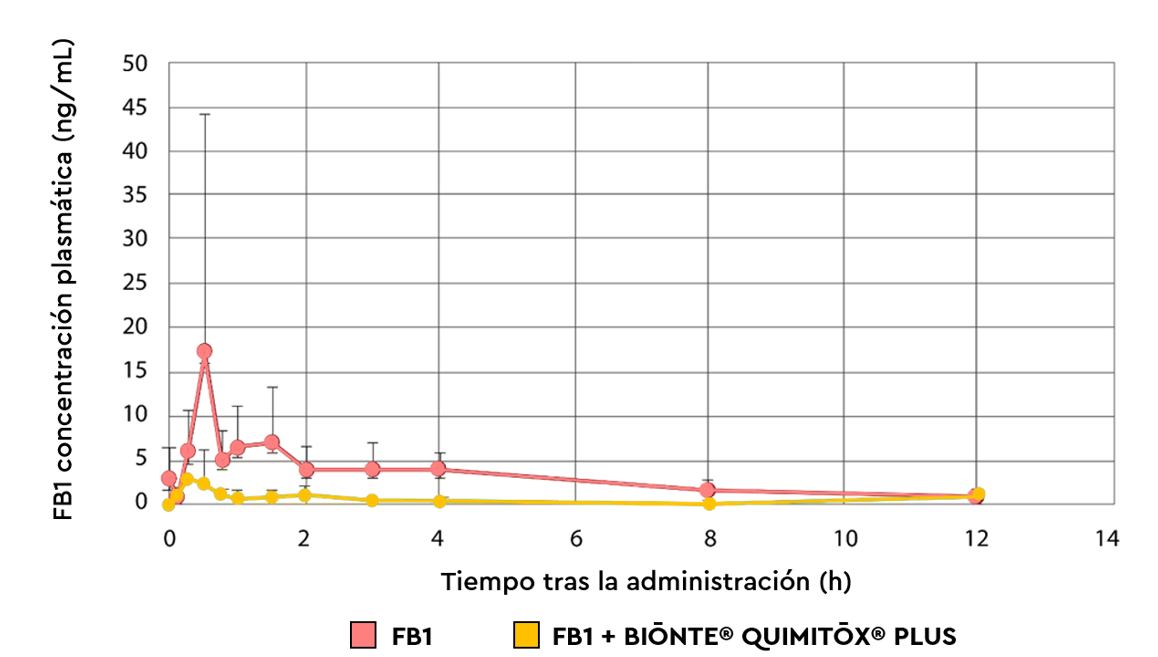
Figura 1: Perfil de concetración plasmática de FB1 en función del tiempo, después de la administración de un bolo oral de 2,5 mg FB1/kg, con y sin BIŌNTE® QUIMITOX® PLUS® (3g/kg de peso vivo).
Siguiendo esta evaluación de eficacia de BIŌNTE® QUIMITŌX® PLUS, un ensayo in vivo realizado en colaboración con el Instituto Samitec y la Universidad de Santa María (Brasil), monitorizó el ratio esfinganina/esfingosina, reconocido biomarcador de exposición a las fumonisinas, en pollos de engorde expuestos a FB1. En este caso, se reportó una reducción del 3,8% en este parámetro de referencia, pudiéndose afirmar que el producto es altamente eficaz frente a las fumonisinas (EFSA, 2010, 2018; Guerre et al., 2022).
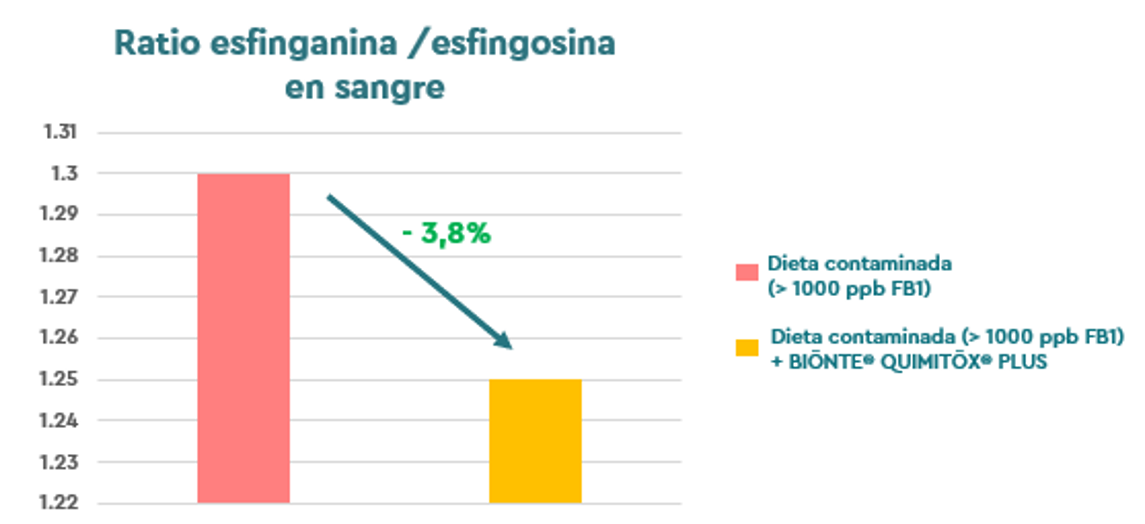
Figura 2: Ratio esfinganina/esfingosina en pollos de engorde expuestos a FB1, y a FB1 + BIŌNTE® QUIMITŌX® PLUS.
Dentro de este mismo ensayo, BIŌNTE® QUIMITŌX® PLUS mejoró el rendimiento productivo de los pollos de engorde expuestos a la dieta contaminada. Se reportó un incrementó en el peso corporal (+0,7%), la ganancia diaria promedio (+2,9%) y la superficie de absorción intestinal (+14,6%), parámetros alterados por la exposición a fumonisinas. Asimismo, el producto redujo el peso relativo del hígado de los animales (-6,1%), indicativo del alivio de los efectos inflamatorios de estas micotoxinas (+12,9%), lo que contribuyó a mantener la integridad hepática en los pollos de engorde expuestos a FB1(Figura 3).
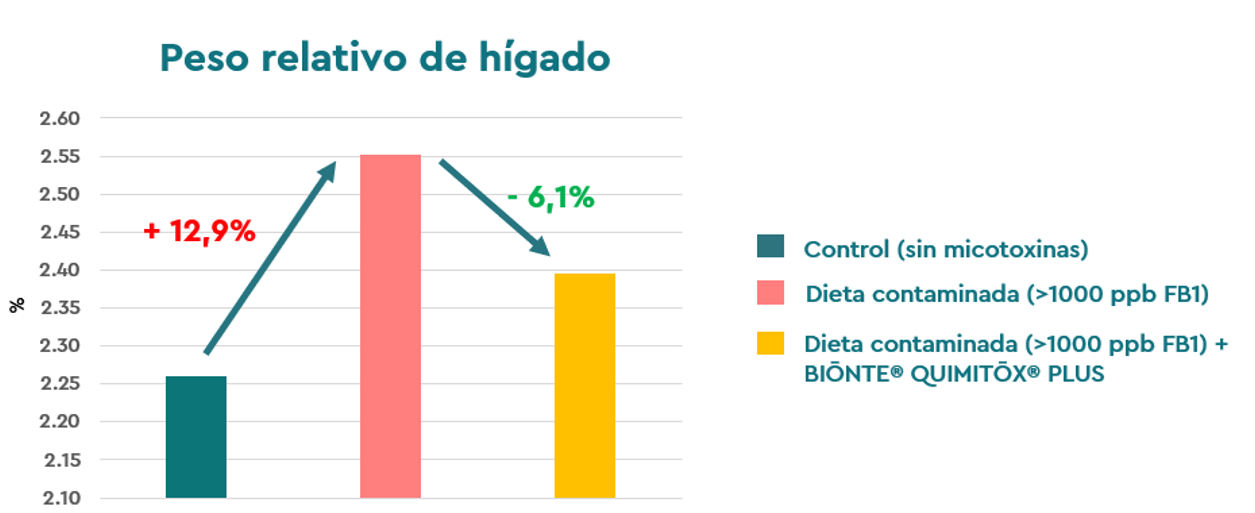
Figura 3: Peso relativo del hígado en pollos de engorde no expuestos a micotoxinas, expuestos FB1 y expuestos FB1 + BIŌNTE® QUIMITŌX® PLUS.
Por otro lado, la eficacia de BIŌNTE® QUIMITŌX® PLUS en gallinas ponedoras expuestas a fumonisinas fue testada, dada la importancia de los efectos de las micotoxinas en esta categoría productiva. Para ello, se realizó un estudio de campo de México, en un grupo de gallinas expuestas a una dieta contaminada naturalmente por fumonisinas, además de AFB1 y deoxinivalenol (DON). El ensayo mostró mejoras significativas en el desempeño productivo, con una reducción en el índice de conversión alimenticia (-5,8%) y un aumento en el porcentaje de huevos comercialmente aptos (+2,7%). Por otro lado, se observó una disminución del 0,25% en la mortalidad y mejoras en la salud hepática confirmadas mediante necropsias.
Conclusión
De esta manera, BIŌNTE® QUIMITŌX® PLUS demostró su efectividad frente a las fumonisinas, un grupo de micotoxinas altamente prevalente a nivel mundial y conocido por sus efectos negativos en la salud y el rendimiento de diversas especies animales. Estas micotoxinas, presentes comúnmente en cereales y subproductos vegetales de la alimentación, pueden afectar órganos clave como el hígado, el sistema inmune y el tracto digestivo, provocando pérdidas productivas importantes.
Los estudios in vitro e in vivo mostraron que la suplementación con BIŌNTE® QUIMITŌX® PLUS no solo mitigó los efectos tóxicos de las fumonisinas, sino que también mejoró parámetros productivos, además de favorecer la salud hepática e intestinal. Estos resultados confirman que BIŌNTE® QUIMITŌX® PLUS es una herramienta confiable para proteger la salud animal y optimizar el desempeño productivo frente a la presencia de fumonisinas.


